|
|
作者:苏增留,PhD, DABCC, FACB
疼痛给人们的日常生活造成很大的影响。但很多人都忽略了慢性疼痛是一种疾病。一般来说,如果疼痛持续一个月以上,并且找不到造成疼痛的原因,医生应该考虑按照疼痛疾病来治疗。在全世界范围内,疼痛的发病率约为35%-45%,在60岁以上的老年人中甚至达到50%以上 [1] 。
疼痛治疗的一个主要的措施就是服用止疼药。而绝大多数的处方类止疼药都是鸦片制剂(opiats)或者鸦片类(opioids)麻醉品,服用不当会造成药物依赖甚至有生命危险。据报道,仅在2010年,美国有15323女性是因为过量服用药物而死亡,其中6631人死于过量服用鸦片类的止疼药。从1999年到2010年,这个数字增加了151.3% [2]。在另一方面,因为这些处方类药物有麻醉和致幻的作用,在黑市上能以较高的价格卖出,有的患者(或者假装的患者)会在同一时期去看不同的医生(doctor shopping),以获得更多的处方类疼痛药。
因此,对正在治疗中的疼痛病人进行药物监测很有必要。在美国,有很多专业的疼痛门诊和疼痛治疗医生,在第一次看病人的时候,病人会被要求和医生签订一个协议,主要内容包括:1)病人不允许再去找另外的医生开药;2)病人只能服用自己的医生开的疼痛药;3)病人不能把自己的疼痛药给其他人(包括出售)。如果医生发现这个协议没有被遵守,处方就会被终止。传统上,这个协议主要基于医生和患者的互相信任,有的医生也会要求病人定期把药瓶带到诊所清点药物的数量。但这种方法费时费力,而且不准确。随着检验技术的发展,现代的临床实验室能够提供客观、准确、并且快速的药物检测结果。疼痛治疗医生也越来越多地依赖临床实验室对其患者进行监测。病人会被要求定期检测尿液中的药物浓度。同时,疼痛病人往往也是使用违禁药物(毒品)的高发人群,除了对开出的处方药物进行监测外,很有必要同时检测常见的违禁药物。研究表明:在美国高达45%的病人没有遵守医嘱。其中20%的病人同时使用如大麻,可卡因,安非他明等其他麻醉品;14% 的病人同时使用了其它来源的疼痛药;10%的病人没有服药;10%的病人在同时看不同的医生,以获得更多的疼痛药物 [3, 4]。
尿液中的药物监测
尿液是最常见的用来监测药物的样本,和血液相比,它有更多的优势:1)采样成本低、方便、并且样本的处理及运输相对简单;2)有更长的药物检测周期,也叫窗口期;3)对病人安全、没有静脉采血的痛苦,同时也降低了医护人员对血源性传染病的接触。在临床实验室中,对疼痛病人主要监测以下几类药物[5-7]:
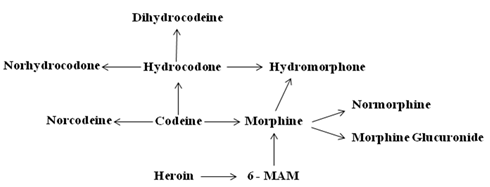
1. 鸦片类制剂(Opioids):包括自然产生的生物碱(也称为Opiats)如可待因(codeine)和吗啡(morphine)和人工合成的具有相似化学结构的衍生物(Opioids),如美沙酮(methadone),海洛因(heroin),氧可酮(Oxycodone),氢可酮(hydrocodone),芬太尼(fentanyl)等。此类药物主要用于止痛,镇咳,止泻等。同时,鸦片类药物能刺激中枢神经系统,让人放松并能产生幻觉,因此容易造成依赖并滥用。海洛因和可待因均属于药物前体(predrug) 进入人体后通过代谢生成有活性的吗啡。其中,海洛因在代谢中可以生成一个独有代谢产物: 6-monoacetylmorphine (6-MAM),因此测定6-MAM可以确定病人是否使用了海洛因(图一)。因为没有临床应用价值并且由于它的危害性,海洛因被划分为一类控制药物。其它具有临床应用价值、但容易造成药物倚赖而必须控制使用的被划分为二类控制药物 [8]。
图一:主要吗啡类药物的代谢产物。(图中可以看出,有些药物同时也是另外一种药物的中间代谢产物,如morphine 和hydrocodone等,因此在分析药物化验报告的时候要了解病人的服药历史)。
质谱仪在成瘾性药物监测中的应用
2. 安非他明/苯丙胺类药物(Amphetamines):包括安非他明(amphetamine),甲基安非他明(methamphetamine))以及它们的衍生物。甲基安非他明的盐酸盐,其结晶如细碎冰块,又因为它的极大危害性,又称为冰毒。安非他明类药物能够刺激神经系统,使人兴奋、警觉、降低疲劳感,并能产生幻觉。此类药物能降低食欲,因此曾经被用作减肥药。安非他明被划分为二类控制药物 [8]。
3. 大麻类(Cannabinoids):在大麻类植物中,至少有61种有类似作用和结构的成分被发现,其中最主要成分是phytocannabinoid ∆9-tetrahydrocannabinol (THC)。THC在尿液中排出的最主要代谢产物是11-nor-∆9- tetrahydrocannabinol-9-carboxylic acid (THC-COOH)。检测THC-COOH通常被用来确定病人是否使用了大麻。因为没有认可的医用价值,并且由于它的成瘾性,大麻类也被划分为一类控制药物 [8]。
4. 可卡因(Cocaine):在手术中可以用作麻醉剂。属于二类控制药物 [8]。在体内,可卡因快速代谢生成芽子碱甲酯(ecgonine methyl ester/EME)和苯甲酰芽子碱(benzoylecgonine/BE)。临床实验室中,对可卡因的监测大多是通过测定尿液中的BE浓度来实现。
5. 苯环己哌啶(phencyclidine/PCP): 俗称天使粉。是一种较强的致幻剂。没有临床应用价值,因此属于一类控制药物。
测定方法
1. 筛选试验 (Screening Tests)
绝大多数的药物筛选试验都是抗原抗体相结合的免疫学方法(immunoassay)。因为快速、简便,并且商业化的试剂基本都可以在临床实验室目前的各种自动分析仪上直接使用,因此对于常规的临床实验室来说,免疫学方法依然是首选。但另一方面,交叉反应(cross-reactivity) 是免疫学方法不可避免的一个缺点。由于抗体会和有相似结构的其他药物或者代谢产物结合,从而产生假阳性反应。比如测定安非他明的试剂除了可以和安非他明以及甲基安非他明发生反应外,还会和麻黄素(ephedrine)或者假麻黄素(pseudoephedrine)结合使检测结果呈阳性。另外,有的免疫反应不能确定具体的药物,只能提示属哪一类药物。例如用于测定鸦片制剂(Opiats)的抗体主要是和吗啡药物分子结合,可待因(codeine)和吗啡(morphine)的使用者都能使反应呈阳性。同时,因为具有相似的结构,很多人工合成的吗啡类药物(opioids)诸如氧可酮(oxycodone),氢可酮(hydrocodone)或者丁丙诺非(buprenorphine)都会与其发生交叉反应。因此在解释结果的时候要仔细询问病人的用药历史。和其它免疫反应不同,用于检测可卡因的抗体特异地和其主要代谢产物BE结合,很少和其它成分发生交叉反应[9, 10]。
另外,每种药物都有一个半衰期(half-life),因此只能在一定的时间内检测得到,也就是检测的窗口期,例如用于确定海洛因的中间代谢产物6-MAM只有 4-8小时的窗口期[5, 6]。解释结果的时候要考虑到尿液的收集时间(表1)。
表一:常见药物的检测窗期
质谱仪在成瘾性药物监测中的应用

综上所述,要谨慎的解释筛选试验的结果。除了结合病人的用药历史,各种药物的检测窗口期也很重要。如果结果和预期的不一样,例如:1)处方上的药物成阴性结果;2)没有在处方上的药物呈阳性结果,医生有必要要求病人进一步作确定试验。
2. 确定试验 (Confirmation Tests)
居于目前的检测技术,气相色谱-质谱(GC-MS)或者液相色谱-质谱(LC-MS)依然是临床上测定尿液中药物的 “金标准”。质谱仪是通过测定 “质量/电荷”(m/z)比来定量或者定性待测分子。因此,在进入质谱仪的分析器(analyzer)之前,任何待测分子都必须首先进行离子化(ionization)。离子化过程对杂质比较敏感,因此待测样本(如尿液或者血清)需要进行前期处理,尽量去掉除待测物之外的其他杂质。色谱(包括气相和液相色谱)能对样本中的各个成分进行很好的分离,而质谱仪能根据“m/z”来测定目标分子,有极高的特异性。因此色谱(LC/GC)和质谱(MS)联用是“强强”联合,是目前能获得的技术中公认的最好的测定方法。
因为气相色谱只适合于能被气化,或者衍生化以后能够气化的小分子,其在临床实验室中的应用比较局限,并且正在被液相色谱-质谱(LC-MS)所取代。以下以LC-MS为例,简单介绍一下临床实验室中的质谱仪使用特点及重点注意事项:
1) 样本的处理:临床实验室的样本主要是血清/血浆和尿液,含有高浓度的蛋白质等其它物质,这些物质会影响离子化效率并且干扰测定,即所谓的基质效应。因此在进入到LC-MS 之前,需要对样本进行提取、纯化、和分离,尽可能多地去掉除待测物以外的其他杂质。目前临床实验室常用的样本处理办法有[11, 12]:
a. 蛋白质沉淀(protein precipitation):是最简单实用的办法,把蛋白质变性沉淀后离心,上清液可以直接进样;或者吹干后再复溶进样,以达到浓缩的目的。但这种方法只能除去大部分蛋白质,其他杂质或者盐类依然会产生基质效应。实际应用中这种方法往往和其他纯化方法联合使用。
b. 液相提取法(liquid-liquid extraction):对样本有极佳的纯化效果,但操作过程相对复杂,并且难以自动化。药物分析中最常见的是用正己烷和乙酸乙酯萃取后分离纯化。
c. 固相提取法(solid phase extraction): 采用固相的吸附剂,待测药物等小分子会被固定在吸附剂上,其他杂质被冲洗掉。目标分子可以再次洗脱下来。可以获得针对目标分子的各种商业化产品,操作简单,纯化效果好,但成本较高。
d. 在线固相提取法(online solid phase extraction):是质谱分析的发展方向。整个样本的纯化过程和LC-MS/MS整合在一起,“在线”完成。样本直接或者简单稀释后上样(dilute and shoot),基本实现了检测过程的全自动化。本文中的例子就是使用这种系统(见下)。
2) LC-MS/MS:液相色谱-双质谱(LC-MS/MS)联用是目前大多数实验室的标准配置。双质谱联用有很高的特异性。通过“选择离子监测”(selected ion monitoring)模式,第一质谱可以只让有特定m/z的“父”或者“前体”离子(parent/precursor ion)通过,在这一过程中,可能有不同的前体离子具有相同的m/z,第一个质谱仪并不能把它们分开。前体离子进入到“碰撞室”(collision center)后,在高能量的作用下化学键断离产生多个“子”或者“产品”离子(daughter/product ion)。第二质谱用于检测待测物特有的“产品”离子,大大增加了双质谱联用的特异性。值得强调的是,药物确定试验一般要求至少检测到两个或两个以上“产品”离子,一个用于定量(quantifier ion),其它用于定性 (qualifier ion)。另外,质谱仪也可以用扫描(scan)模式来监测所有的离子。
3) 一般来说,在尿液中同时检测到药物和其代谢物是确定病人服药的主药指标。如果病人没有服药,而是在收集尿液时把药物加进去,这种情况下检测不到代谢产物。
4) 基质效应是影响质谱仪的一个重要因素,其中对离子化过程的影响尤其重要。基质效应可以抑制(ion suppression)或者加强(ion enhancement)离子化过程,但最常见的是前者。因此,所有新建立的基于质谱仪测定的方法,都要求对基质效应进行评价。有多种方法可以用于评价基质效应,临床上常用的有两种[13-15]。
5) 按照CLIA和CAP的要求,所有没有被FDA认证的方法都必须建立并确证(validation)以下参数:a)精密度(precision);b)准确度(accuracy);c)线形范围(linearity);d)最小检测限(limit of detection/LOD;limit of quantification/LOQ); e)干扰(interference)。
除了具有很高的特异性和灵敏度,质谱方法另一个最大的特点就是可以同时测定多个待测物(analytes)。Yuan et al 等人建立了一种基于LC-MS/MS的方法,通过测定尿液中19中分子(包括药物及其代谢产物)来监控15种常见药物[16]。以下对此方法做一些介绍:
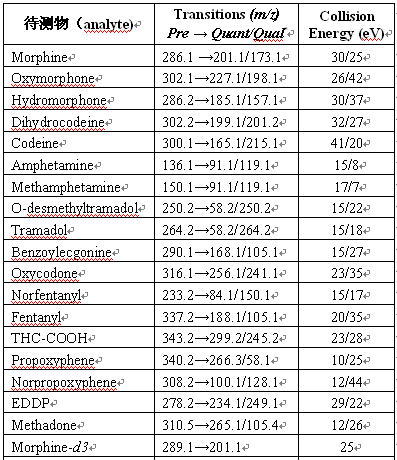
1) 待测药物(analytes):吗啡(morphine,同时也是可待因的活性中间代谢产物),双氢可待因(dihydrocodein),氧可酮(oxycodone),氧吗啡酮(oxymorphone),氢可酮(hydrocodone),氢吗啡酮(hydromorphone),美沙酮(Methadone)及其代谢产物EDDP,芬太尼(fentanyl)及其代谢产物norfentanyl,曲马多/反胺苯环醇(tramadol)及其代谢产物氧去甲基曲马多(O-desmethyltramadol),丙氧酚(propoxyphene)及其代谢产物norpropoxyphene,安非他明(amphetamine),甲基安非他明(methamphetamine),可卡因的代谢产物BE,大麻的代谢产物THC-COOH。表二显示了各个待测物的主要参数。大多数临床实验室中的质谱仪使用的都是电喷射离子化法(electrospray ionization),即让待测物“质子化”(protonization),因此对不同的系统 “前体”离子(parent ion or precursor ion)应该都是一样的,但 “产品”离子(daughter ion or product ion)与碰撞室的能量和撞击方式有关,不同的系统可以完全不一样。因此在参考的时候要结合自己实验室的质谱系统作具体分析。
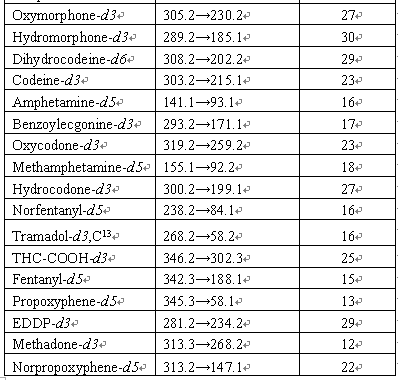
2) 内标(Internal Standard):氘或者C13标记。表二中详细的列出了各个内标物的参数。
表二:MS/MS 主要参数。(注解:*前体离子→定量离子/定性离子)
质谱仪在成瘾性药物监测中的应用
质谱仪在成瘾性药物监测中的应用
3) 样本的初步处理——水解:和其他常见的检测方法不一样,绝大多数的药物经过体内代谢后,都会葡糖醛酸化(glucuronidation),以增加水溶性而使药物容易排除体外。因此,为了准确测定待测物的浓度,一般情况下需要通过水解去除葡萄糖苷酸。本例中使用葡糖苷酸酶: 0.2mL 尿液和0.1 mL 的内标液混合后再加入0.1 mL新鲜配制的葡糖苷酸酶,60摄氏度过夜。水解后的样本再和0.4 mL的水/甲醇混合物(1:1)混合后直接上样。
4) 液相色谱(LC):ThermoFisher 的Transcend TLX-1 系统。正如前文所述,此系统属于“在线固相提取法”。简单来说,此系统有两套“色谱柱”系统。第一套称之为“湍流柱”(TurboFlow Column)。此类柱子装有大颗粒的填充物,使用水作流动相。在高流速的情况下(1.5-5.0 mL/min)产生湍流,小分子会滞留在颗粒的孔洞中,蛋白质等大分子物质会被直接冲洗到废液管里。与之相连的第二套柱子也叫“分析柱”(analytical column),即相当于正常的液相色谱柱,对纯化后的产物进一步进行分离,然后进入质谱仪 [17]。
5) 双质谱(MS/MS):Thermofisher 的TSQ Quantum UltraTM triple quadrupole mass spectrometer。其本质就是最常见的两个偶联的四极质谱(quadrupole),中间有一个碰撞室 (collision center)。主要参数: a) spray voltage: 4000 V; b) vaporizer temperature: 350 ℃; c) sheath gas pressure: 50 units; d) auxiliary gas pressure: 25 units; e) ion sweep gas pressure: 2 units; f) capillary temperature: 275 ℃; g) collision gas pressure: 1.5 mTorr; h) 第一和第二质谱的分辨率(resolution): 0.7 m/z。其他参数见表二。
结束语
很多人没有意识到,在某种程度上对处方药的滥用比对毒品的滥用情况更严重,尤其在青少年中。在美国,有超过一千五百万的人在滥用处方药,这个数字远比滥用可卡因,海洛因等致幻剂的总合还要高。很多人滥用处方药是因为这些药比毒品更容易获得,另外,他们觉得处方药更“安全”。但事实是:2005年,在美国有22400人因为药物滥用死亡,其中45%是服用过量的处方药,其中止疼药(pain killer)占了38.2% [18]。
除了成瘾性药物,一些毒性比较大的治疗药物的使用也需要严格监测,如免疫抑制剂(Immunosuppressants)。因为血药浓度对治疗效果和毒性的判断很重要,所以此类药物一般是检测血液样本。在临床实验室中,药物的监测首选依然是免疫学方法。最主要的原因就是快速、简便 。质谱是药物检测的“金标准”,但以下几个原因限制了其在临床实验室中的广泛应用:1)投入资本(所谓“capital”)太高。一台质谱系统花费动辄数10万美元。因为不需要特别的试剂,质谱生产厂家不愿意象大多数的全自动生化分析仪那样通过使用一定量的试剂来免费租用仪器;2)需要专门的维护人员。因为有很高的灵敏度和特异性,仪器需要随时有专门的技术人员维护;3)缺少熟练的操作人员;4)自动化程度相对较低,需要对样品进行前期处理。但随着质谱仪灵敏度和分辨率的提高,再加上在线固相提取技术的进步,质谱系统的全自动化将会实现。一般来说,对已经拥有了质谱系统的实验室来说,都想最大限度的使用质谱,除了高灵敏度和高特异性外,另一个很大的原因就是极低的试剂成本。
参考文献
[1] 李颖,喻京英. 慢性疼痛也是病. 人民日报海外版2013.
[2] Mack KA. Drug-induced deaths - United States, 1999-2010. MMWR Surveill Summ 2013;62 Suppl 3:161-3.
[3] Michna E, Jamison RN, Pham LD, Ross EL, Janfaza D, Nedeljkovic SS, et al. Urine toxicology screening among chronic pain patients on opioid therapy: frequency and predictability of abnormal findings. The Clinical journal of pain 2007;23:173-9.
[4] Ives TJ, Chelminski PR, Hammett-Stabler CA, Malone RM, Perhac JS, Potisek NM, et al. Predictors of opioid misuse in patients with chronic pain: a prospective cohort study. BMC health services research 2006;6:46.
[5] Moeller KE, Lee KC, Kissack JC. Urine drug screening: practical guide for clinicians. Mayo Clinic proceedings 2008;83:66-76.
[6] Christo PJ, Manchikanti L, Ruan X, Bottros M, Hansen H, Solanki DR, et al. Urine drug testing in chronic pain. Pain physician 2011;14:123-43.
[7] Reisfield GM, Salazar E, Bertholf RL. Rational use and interpretation of urine drug testing in chronic opioid therapy. Annals of clinical and laboratory science 2007;37:301-14.
[8] DEA. Drug Schedules. http://www.justice.gov/dea/druginfo/ds.shtml.
[9] Heit HA, Gourlay DL. Urine drug testing in pain medicine. Journal of pain and symptom management 2004;27:260-7.
[10] Reisfield GM, Goldberger BA, Bertholf RL. 'False-positive' and 'false-negative' test results in clinical urine drug testing. Bioanalysis 2009;1:937-52.
[11] Yuan C, Chen D, Wang S. Drug confirmation by mass spectrometry: Identification criteria and complicating factors. Clinica chimica acta; international journal of clinical chemistry 2014.
[12] Xu RN, Fan L, Rieser MJ, El-Shourbagy TA. Recent advances in high-throughput quantitative bioanalysis by LC-MS/MS. Journal of pharmaceutical and biomedical analysis 2007;44:342-55.
[13] Dams R, Huestis MA, Lambert WE, Murphy CM. Matrix effect in bio-analysis of illicit drugs with LC-MS/MS: influence of ionization type, sample preparation, and biofluid. Journal of the American Society for Mass Spectrometry 2003;14:1290-4.
[14] Annesley TM. Ion suppression in mass spectrometry. Clinical chemistry 2003;49:1041-4.
[15] Taylor PJ. Matrix effects: the Achilles heel of quantitative high-performance liquid chromatography-electrospray-tandem mass spectrometry. Clinical biochemistry 2005;38:328-34.
[16] Yuan C, Heideloff C, Kozak M, Wang S. Simultaneous quantification of 19 drugs/metabolites in urine important for pain management by liquid chromatography-tandem mass spectrometry. Clinical chemistry and laboratory medicine : CCLM / FESCC 2012;50:95-103.
[17] Christophe Chassaing SR. Turbulent flow chromatography: an evolving solution for bioanalysis. Chromatography today 2009.
[18] The truth about prescription drug abuse.http://www.drugfreeworld.org/drugfacts/prescription/abuse-international-statistics.html. |
|
 |关于我们|医维基|网站地图|Archiver|手机版|医疗之家
( 沪ICP备2023001278号-1 )
|关于我们|医维基|网站地图|Archiver|手机版|医疗之家
( 沪ICP备2023001278号-1 )