|
作者:复旦大学附属中山医院检验科 郭玮, 潘柏申
丙型肝炎病毒(hepatitis C virus,HCV)感染已成为严重的公众健康问题之一。据估计,全球范围内约有1.7~2亿人感染HCV[ 1]。美国疾病控制与预防中心(Centers for Disease Control and Prevention,CDC)报道美国有320万慢性感染患者,已成为了美国最常见的肝移植原因。而我国感染人数已超过4 000万,占全世界感染人数的1/4,在未来20年内,与HCV感染相关的死亡率(肝衰竭及肝细胞肝癌导致的死亡)将急剧增加[ 2]。
在疾病治疗进展方面,目前已有一些直接抗病毒药物(direct-acting agents,DAAs)获得美国食品和药物管理局(Food and Drug Administration,FDA)批准。此外,虽然有一些治疗性疫苗已经在进行一期或者二期临床研究[ 3],但由于HCV的变异非常频繁,目前为止仍没有任何一种保护性疫苗能够为丙型肝炎患者提供帮助。因此,活动期HCV感染的诊断对于减缓其传播是至关重要的。我们介绍了用于筛查HCV感染以及患者治疗监测的实验室检测项目。
一、HCV传播途径
HCV的传播途径包括经血传播、性接触传播及母婴传播。经血传播主要包括输血和使用血液制品,以及经破损的皮肤和黏膜传播。目前,后者是最主要的传播途径,特别是静脉注射药物(毒品)以及针刺伤。在某些地区静脉注射药物(毒品)导致的HCV感染占60%以上。
二、HCV基因结构
HCV属于黄病毒科,为单链RNA病毒,含有9 400个核苷酸,可编码6~8种蛋白质,在其5’端和3’端各有一个非编码区。见图1。5’端非编码区是主要的病毒核酸检测的靶位点,而血清学检测的是针对c22-3、c33c和c100-3多肽的抗体。
不同病毒株的HCV显示了相当大程度的核酸序列的变异。通过核酸序列比较可将HCV分为6种主要的基因型和至少50种亚型[ 4]。
丙型肝炎诊断及治疗检测中实验室检测项目的应用
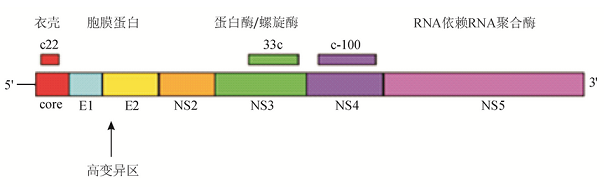 图1 HCV的基因结构
图1 HCV的基因结构
三、HCV检测
抗-HCV抗体检测可用于HCV感染的筛查,推荐进行HCV筛查的人群包括:处于HCV感染高发区的人群、接受输血或器官移植者、针刺伤或粘膜暴露于HCV阳性血液的医疗卫生工作人员、怀疑存在母婴传播、静脉吸毒者、性伴侣HCV阳性者[ 5]。
目前为止,抗-HCV抗体酶免法(enzyme immunoassays,EIAs)检测已经历了3代的发展。第1代方法以单一重组病毒蛋白(C100-3)作为抗原,相当于NS3的一部分和几乎全部NS4基因的产物,仅代表整个HCV抗原的一小部分(12%),灵敏度较低。第2代试剂以2种非结构蛋白(NS3/NS4重组蛋白)作为抗原,并增加了一种核心区蛋白(C22-3)。与第1代方法相比较,第2代方法同时具备HCV结构区和非结构区两部份抗原,使灵敏度和特异性都有进一步提高。第3代方法在第2代试剂抗原的基础上,适当增加了C33c在整个抗原中的比重,进一步提高了早期诊断的灵敏度。
图2为美国CDC推荐的完整的抗-HCV抗体筛查和血清学补充确认试验的报告策略。可见,补充确认试验如重组免疫印迹法对于S/CO比值高于95%阳性预测值的患者标本而言不一定是必须的。例如较早的研究提示,用EIAs检测健康志愿者样本,吸光度值/Cut-off值(signal-to-Cut off,S/CO)的比值>均值能够用来预测补充确认试验的阳性结果[ 6]。随后,其他人群的研究进一步证明了S/CO值有95%的阳性预测值,且与不同人群及其发病率无关。对于EIA,筛查结果的S/CO值>3.8可预测重组免疫印迹法(recombiant immunoblot assay, RIBA)检测结果阳性(准确性>95%);对于化学发光方法(chemiluminescent immunoassays,CIAs),由于阳性筛查范围要比EIA大。因此,大多数实验室使用S/CO值>8。但需注意,不同的初筛试剂性能不同,S/CO比值的判断标准会有所不同。
EIAs和CIAs检测HCV抗体的特异性均>99%。HCV核酸检测(nucleic acid tests,NATs)也被称为HCV RNA检测或转录介导的核酸扩增检测同样有非常高的特异性。FDA认证的NATs方法应该被用于判断抗-HCV抗体阳性的患者是否处于病毒感染的活动期。
美国CDC建议在对丙型肝炎患者进行首次治疗前,应先进行HCV的基因分型,基因分型结果可帮助临床医生制定治疗方案(药物剂量和治疗周期)以及估计疗效。相较于2型和3型基因型,我国发病率最高的1型基因型对干扰素的反应较差,也需要更长时间的治疗。但在1型患者中,宿主 IL28B基因型被认为是对二联或三联疗法有持续病毒应答(sustained virological response,SRV)的治疗前预测指标[ 7]。
有研究报道了高病毒载量的患者组其肝功能指标丙氨酸氨基转移酶(alanine aminotransferase,ALT)、天门冬氨酸氨基转移酶(aspartate aminotransferase,AST)、直接胆红素等高于低病毒载量患者。因此,肝功能指标也能辅助临床对病毒感染的严重程度作出判断[ 8]。
丙型肝炎诊断及治疗检测中实验室检测项目的应用
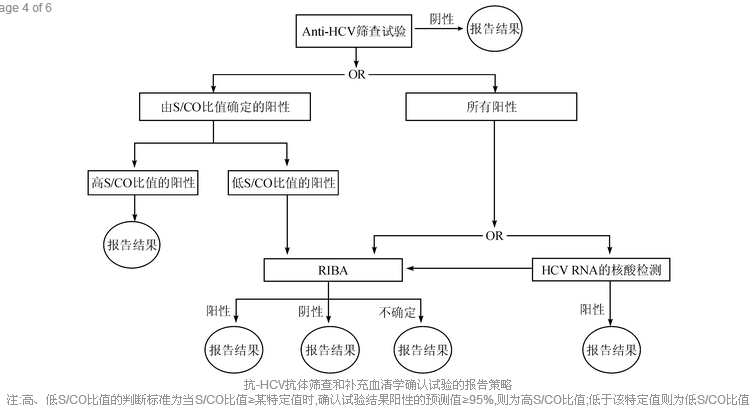 图2 抗-HCV抗体筛查和补充血清学确认试验的报告策略
图2 抗-HCV抗体筛查和补充血清学确认试验的报告策略
注:高、低S/CO比值的判断标准为当S/CO比值≥某特定值时,确认试验结果阳性的预测值≥95%,则为高S/CO比值;低于该特定值则为低S/CO比值
四、肝活检
内科医生治疗慢性丙型肝炎患者一般不根据组织学检查结果及患者可能的感染时间长短来定制治疗方法。肝活检提供了肝脏损伤程度及其他有用的信息,有助于医生决定随访及治疗。例如,肝活检的结果提示肝纤维化或硬化的程度,后者需要进一步监测肝癌的发生和/或检查有无胃底静脉曲张。
然而肝活检结果还不够理想。因为活检样本只是肝组织的很小一部分并且采样部位可能不是病变最严重的区域。此外,肝活检具有不能忽视的风险(虽然发生概率很小),例如出血和胆汁性腹膜炎等。
肝活检是评估HCV感染的金标准,但如今已受到了质疑。已有的无创检测技术以及其他一些技术正在被评估,希望有朝一日能够取代肝活检。
五、治疗方案
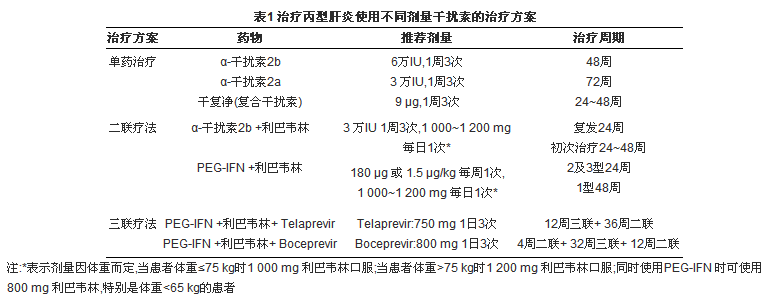
不同的慢性丙型肝炎感染的治疗方案都是建立在干扰素、聚乙二醇干扰素(pegylated interferon,PEG-IFN)以及利巴韦林的各种组合的基础上,可以单药或二联治疗(具体组合见表1)。2011年,FDA批准了2种蛋白酶抑制剂——Boceprevir和Telaprevir用于治疗1型丙型肝炎。这些新的DAAs是慢性丙肝治疗上的重大突破,甚至可能改变治疗标准。增加其中一种药物到二联疗法中能够产生显著的病毒持续应答,被称为三联疗法[ 9]。
丙型肝炎诊断及治疗检测中实验室检测项目的应用
六、治疗反应的预测
表2列出了HCV治疗反应的预测指标。
丙型肝炎诊断及治疗检测中实验室检测项目的应用
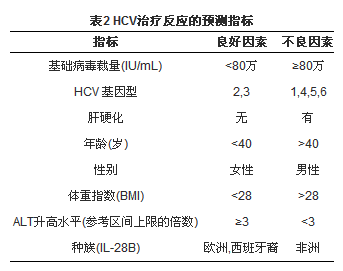
1.基础病毒载量 基础病毒载量是公认的治疗反应预测指标。基础病毒载量<80万IU/mL的患者具有更好的治疗反应[ 10]。此外,定量HCV RNA分析能检测出更低病毒载量的患者。这些患者有机会取得更持久的治疗反应。医生一般在最初治疗前检测病毒载量用于了解HCV感染程度,便于为患者分析治疗的风险和益处。此外,这也能提供患者的基础病毒载量水平以衡量治疗期间病毒载量下降的程度。
2.HCV基因型 不同的研究都表明基础病毒载量不是影响干扰素治疗的单一因素。一些研究证明不同的HCV基因型对于治疗的反应存在明显差异。引起差异的原因还不清楚,但是不同基因型病毒的复制效率存在差异,从而引起不同的血清病毒水平和对干扰素的响应[ 10, 11]。另外,一些研究也提示病毒的干扰素抵抗存在遗传学基础。总而言之,HCV 1型、4型和5型的患者对干扰素的反应较2型和3型的患者不敏感。
3.宿主 IL28B基因型 除了病毒基因型,宿主遗传学因素在感染过程中似乎也起了作用。最近的研究发现在19号染色体干扰素L3(interferon lambda 3)基因附近的特异性多态性( IL28B)具有明显的自发病毒清除能力。研究显示在自发病毒清除而非发展成慢性肝炎的患者中,rs12979860位点的CC型人群比例是普通人群比例的2倍。 IL28B多态性也显示出对于治疗效果的影响。研究也证明了 IL28B基因型对SRV的预测价值要优于其他几种因素,包括基础HCV RNA水平、纤维化程度、年龄和性别;且在1型HCV感染患者中的预测价值要高于2型和3型感染患者。其他靠近 IL28B的多态性也能预测SRV,如rs8099917。
七、治疗监测
对于接受二联疗法的患者,实验室应在治疗前和治疗12周后使用相同的定量方法检测HCV RNA水平。早期病毒应答(early virological response,EVR)被定义为在最初的12周治疗后获得大于两个数量级的HCV RNA水平的下降。这种应答是非常有临床价值的。如果没有获得EVR,那么获得SVR的可能性仅>3%。如果治疗的目标仅是获得SVR,那么临床医生会在12周没有获得EVR时停止治疗;但即使没有获得SVR,也可能获得组织学改善,因此有一些临床医生会在12周后继续治疗。
在治疗结束或完整治疗并获得SRV>6个月后监测时,需要更敏感、有更低检出限的检测方法[ 12]。实验室应该谨慎选取HCV RNA检测方法,该方法不仅需要有较大的动态检测范围,也需要有较低的检出限。
图3显示了全面的实验室对HCV感染诊断、预后判断及二联疗法治疗监测随访的检测策略。在开始治疗后,临床医生通过检测患者的HCV RNA水平来判断疗效、鉴定SVR以及了解病毒是否被清除。
八、治疗前景
未经治愈的慢性HCV感染会导致肝硬化、肝癌和肝外疾病。在所有人都能常规接种HCV疫苗或者高危人群能纠正其高风险行为,感染的患者都应该接受治疗干预。干扰素是目前最主要的治疗选择,新的治疗方案仍需在临床研究中进一步评估。
将利巴韦林加入PEG-IFN治疗方案中是慢性丙型肝炎治疗的一大进步。Boceprevir和Telaprevir的应用也是1型丙型肝炎治疗的重要进步。新的和更有效的治疗方案仍需进一步研究,包括针对非1型丙型肝炎的治疗。
丙型肝炎诊断及治疗检测中实验室检测项目的应用
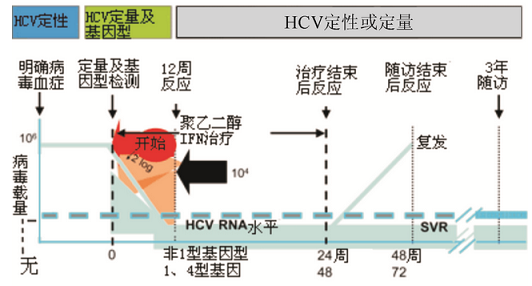 图3 二联疗法检测方案
图3 二联疗法检测方案
参考文献
[1] Williams R. Global challenges in liver disease[J]. Hepatology, 2006, 44(3): 521-526.
[2] Davis GL, Albright JE, Cook SF, et al. Projecting future complications of chronic hepatitis C in the United States[J]. Liver Transpl, 2003, 9(4): 331-338.
[3] Halliday J, Klenerman P, Barnes E. Vaccination for hepatitis C virus: closing in on an evasive target[J]. Expert Rev Vaccines, 2011, 10(5): 659-672.
[4] Simmonds P, Holmes EC, Cha TA, et al. Classification of hepatitis C virus into six major genotypes and a series of subtype by phylogenetic analysis of the NS-5 region[J]. J Gen Virol, 1993, 74(Pt 11): 2391-2399.
[5] 中华医学会检验分会, 卫生部临床检验中心, 中华检验医学杂志编辑委员会. 肝脏疾病诊断治疗中实验室检测项目的应用建议[J]. 中华检验医学杂志, 2013, 36(9): 773-784.
[6] Smith BD, Morgan RL, Beckett GA, et al. Recommendations for the identification of chronic hepatitis C virus infection among persons born during 1945-1965[J]. MMRW Recomm Rep, 2012, 61(RR-4): 1-32.
[7] Ge D, Fellay J, Thompson AJ, et al. Genetic variation in IL28B predicts hepatitis C treatment-induced viral clearance[J]. Nature, 2009, 461(7262): 399-401.
[8] 方超萍, 孙薇薇, 孙小波, 等. 丙型肝炎患者不同病毒载量与病毒学应答及肝功能改变的相关性[J]. 现代检验医学杂志, 2012, 27(5): 18-21.
[9] McHutchison JG, Everson GT, Gordon SC, et al. Telaprevir with peginterferon and ribavirin for chronic HCV genotype 1 infection[J]. N Engl J Med, 2009, 360(18): 1827-1838.
[10] Poynard T, Marcellin P, Lee SS, et al. Rand omised trial of interferon alpha 2b and ribavirin for 48 weeks or for 24 weeks versus interferon alpha 2b plus placebo for 48 weeks for treatment of chronic infection with hepatitis C virus. International Hepatitis Interventional Therapy Group (IHIT)[J]. Lancet, 1998, 352(9138): 1426-1432.
[11] Davis GL, Lau JY. Factors predictive of a beneficial response to therapy of hepatitis C[J]. Hepatology, 1997, 26(3 Suppl 1): 122S-127S.
[12] Dienstag JL, McHutchison JG. American Gastroenterological Association technical review on the management of hepatitis C[J]. Gastroenterology, 2006, 130(1): 231-264. |
 |关于我们|医维基|网站地图|Archiver|手机版|医疗之家
( 沪ICP备2023001278号-1 )
|关于我们|医维基|网站地图|Archiver|手机版|医疗之家
( 沪ICP备2023001278号-1 )