|
作者:李刚,赵梅,周晓燕,贾伟
单位:宁夏医科大学总医院医学实验中心 宁夏临床病原微生物重点实验室
近年来,随着全球范围内耐药细菌的广泛传播,国家卫生和计划生育委员会颁布了我国史上最严的有关抗菌药物的法令––第84号《抗菌药物临床应用管理办法》[1]。法令颁布后,临床微生物检验对临床变得更为重要,同时也促使临床微生物检验工作发生了巨大的变化,其中最重要的是临床微生物室工作重心需要向检验前和检验后倾斜,加强与临床的沟通。本文对在检测前的临床样本采集与运送、检测过程及检测结果报告这几个环节中,应如何加强临床微生物室与临床的协作进行论述。
1 样本的采集与运送
临床样本的规范采集和运送是微生物检验的前提和基础,样本的质量直接关系到检测结果的准确性和可靠性。因此,临床微生物室人员有责任提供详细准确的采集手册供临床参考。微生物培养样本采集除了有检验的通用原则"三查七对",还有三大原则:
(1)无菌操作原则。无菌操作有两个目的,一是在采集过程中避免样本受到环境中或者患者身上正常菌群的污染,比如下呼吸道样本要避免受到上呼吸道(口腔)正常菌群的污染,在取材时最好取肺泡灌洗液、支气管毛刷等不易受到污染的样本,如果是自然咳痰则需要评估;再如皮肤毛囊中存在大量凝固酶阴性葡萄球菌、痤疮丙酸杆菌等正常菌群,采集血培养样本时需要对穿刺点实施三步消毒的步骤,保证消毒充分有效。第二,避免采集人员被感染,来自患者的样本可能含有未知生物危害,采集人员应进行很好的生物安全防护,采集运送的容器应无菌,不易泄露。
(2)抗菌药物使用之前采集原则。有研究表明,如患者在血培养前已使用抗菌药物,培养的阳性率会降低50%~80%[2]。因此,应尽可能在使用抗菌药物之前采集样本,如已经使用抗菌药物,应使用可以吸附或中和抗菌药物的培养基,如加有活性炭或树脂颗粒的,或者在下一次使用抗菌药物之前采集样本,以减少抗菌药物对培养结果的影响。
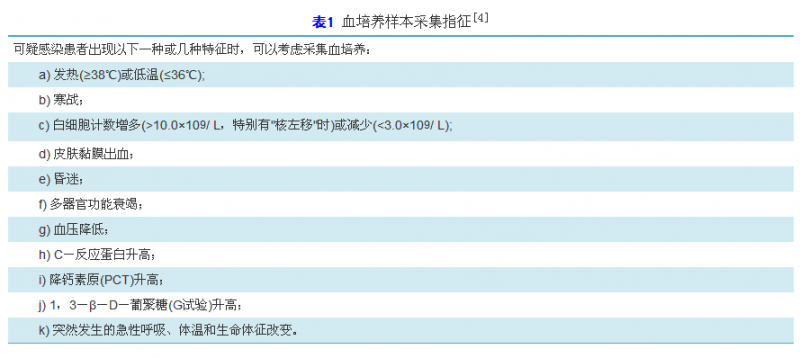
(3)及时运送原则。所有样本都应在采集后2 h内送至微生物实验室。对于含有环境敏感的细菌如志贺菌属(需要立即接种)、淋病奈瑟菌、脑膜炎奈瑟菌和流感嗜血杆菌(对温度比较敏感)等的样本,如脑脊液、生殖道样本、眼部样本、内耳样本不允许冷藏保存。其他样本则可在4℃保存一定的时间。临床医护人员除了要遵循上述微生物样本采集原则外,还应对不同样本的采集指征有所了解,根据采集指征进行样本采集才能使临床微生物检测的阳性率最高。血培养是所有细菌培养中最有意义的,不仅是在诊断菌血症或脓毒血症过程需要,在其他部位感染的多个指南中也都提到了血培养的重要性,如美国感染性疾病协会(The Infectious Diseases Society of America,IDSA)脑膜炎诊断标准[3]中建议,在怀疑细菌性脑膜炎时,无论该患者是否有免疫抑制、中枢神经系统的疾病史、视乳头水肿、局灶性神经功能缺损或者之前做过腰椎穿刺,都应该紧急抽血送培养。
下面以血培养为例,对样本采集的指征和具体要求进行说明(表1)。
加强临床微生物实验室与临床的沟通
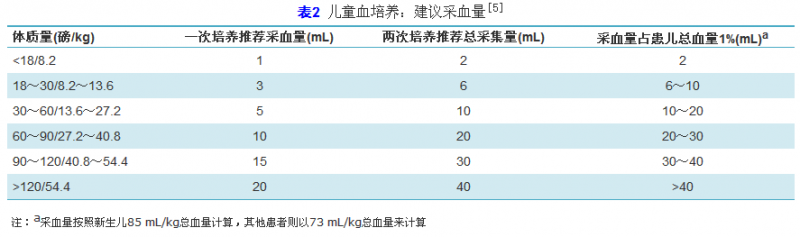
血培养应同时采集2~3套血液样本(每套部位不同),成人每瓶采血量8~10 mL,儿童1~5 mL,但不应超过患儿总血量的1%,新生儿为0.5 mL。临床上,儿童血液样本的采集比成人困难,Kaditis等[5]对儿童血培养的采血量有详细研究(表2)。对于怀疑导管相关血流感染,建议至少送检两套血培养(需氧瓶和厌氧瓶),至少一套为经皮穿刺,取外周血,另一套为静脉导管内取血培养,48 h内新插内导管则不需要进行培养。如果从两套血培养中获得了相同的病原菌,一般可认为该菌为病原菌。此外,如果从导管插管取血进行培养比外周血培养阳性报警时间早2 h或以上,也可作为静脉导管是感染来源的证据[6]。
加强临床微生物实验室与临床的沟通
2 检测过程中沟通
对临床样本进行实验室检测时,如出现与临床医师预判不一致的情况,实验室需要与临床积极沟通。同时临床需向实验室提供与检测相关的信息,如诊断、抗菌药物使用情况、疑似感染类型、体温、怀疑的目标菌等。
2.1 样本的性状
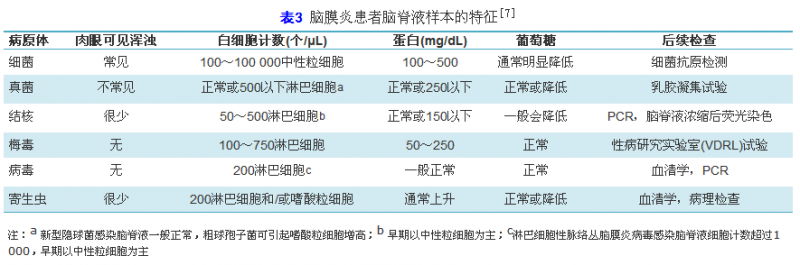
样本性状既可以用来判断样本是否合格,也可以用于感染类型的初步判断。下呼吸道样本中,痰样本必须进行合格性判断,如痰液的性状如唾液,清亮,有大量泡沫存在,该样本不合格。同时,必须结合直接涂片革兰染色镜检结果,低倍镜视野,>25个多形核白细胞,<10个鳞状上皮细胞,这样的样本是合格的。脑脊液样本的性状与感染类型相关,常见脑膜炎主要为病毒型、化脓型(细菌性)和结核型(表3),根据脑脊液的特点,建议临床医师进行后续检查。
加强临床微生物实验室与临床的沟通
2.2 病原菌筛选
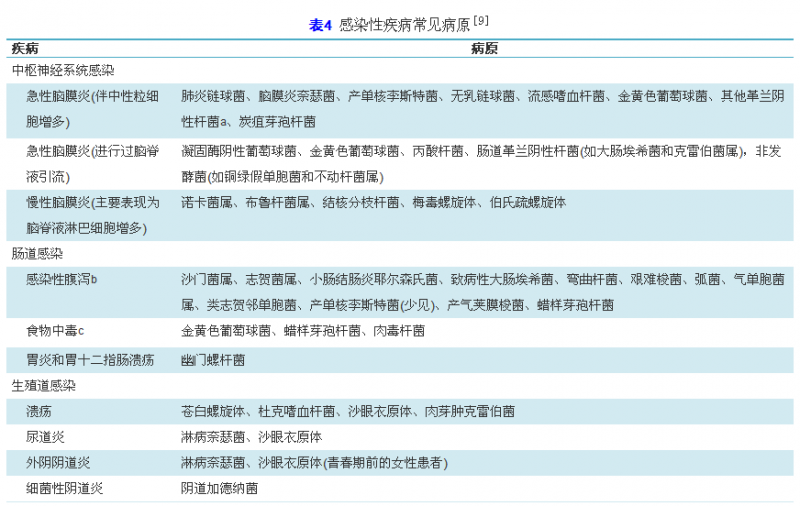
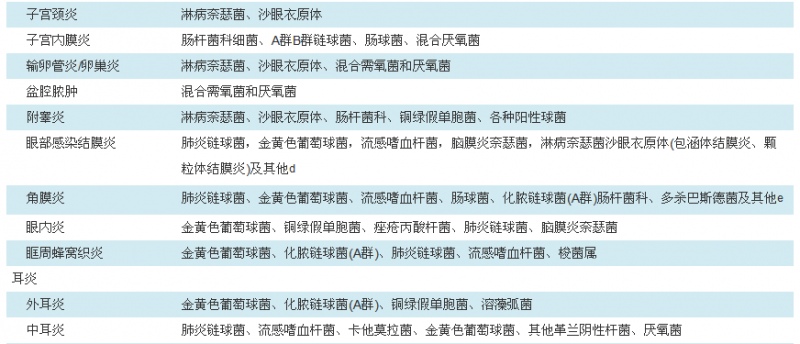
建议实验室人员与临床医师共同制订不同类型感染性疾病的病原菌筛选标准。在进行病原菌筛选时,应结合感染的流行病学资料、感染部位和疾病严重程度等,并应区分医院感染与社区感染。表4是临床常见感染性疾病的常见病原[8],供参考。对于心内膜炎的诊断,改良杜克感染心内膜炎诊断[9]中确诊的主要条件就是血培养阳性,其病原菌大多为上呼吸道定植的正常菌群,必须从两次单独血培养中培养出如草绿色链球菌,牛链球菌,HACEK菌(Haemophilus.嗜血杆菌属、Actinobacillus.放线杆菌属、Cardiobacterium.心杆菌属、Eikenella.艾肯菌属、Kingella.金杆菌属),以及金黄色葡萄球菌这些典型的心内膜炎感染病原菌才能确诊;或者重点考虑社区获得性肠球菌存在;或者多套阳性血培养病原菌一致。这些阳性血培养至少2套采集时间>12 h或者1 h内采集的3次血培养全部阳性,或者4次血培养中3次及以上阳性。单次血培养阳性只对于少数病原(如伯氏考克斯体)有意义。
加强临床微生物实验室与临床的沟通
加强临床微生物实验室与临床的沟通
加强临床微生物实验室与临床的沟通

3 报告单的解释
结果的发布不仅仅是发送报告单,还包括报告在临床应用的咨询以及定期监测数据的发布,这个过程是临床与实验室相互了解和熟悉的过程,对个体化治疗方案的制定至关重要。血液、脑脊液、骨髓、无菌体液等样品的培养鉴定应及时发送分级报告,如样本直接涂片或湿片直接镜检、培养结果的判读等阳性发现[10]。
3.1 报告单的内容
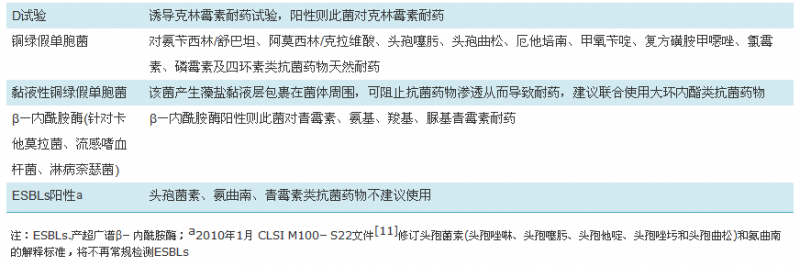
临床微生物实验室的检测报告单一般由两部分组成,一部分是鉴定结果,一部分是药敏结果。我国药敏从试验的操作到结果的判断均参照美国临床实验室标准化协会(Clinical and laboratory standards institute,CLSI)临床微生物的相关标准,试验结果根据试验方法的不同分为抑菌圈直径(纸片扩散法、Kirby-Bauer法)和最低抑菌浓度(MIC,肉汤稀释法、琼脂稀释法、E试验法)。抑菌圈直径是一个定性的结果,只能告诉临床医师抗菌药物的敏感性,不能提供敏感的程度;而MIC不仅有敏感性,还可以告知医师菌株对抗菌药物敏感或耐药的程度。CLSI标准是让临床医师了解药敏的一个很重要的内容,比如敏感(Susceptible)、中介(Intermediate)、耐药(Resistant)的定义,以及在2014年CLSI-M100文件[11]中增加的剂量依赖敏感(Susceptible-dose dependent,SDD)概念。微生物实验室的检测报告单除了提供具体的药敏结果,还要根据不同的细菌提供各种特殊耐药表型,比如耐甲氧西林葡萄球菌(Methicillin resistant Staphylococcus,MRS)、β-内酰胺酶、超广谱β-内酰胺酶(Extended-spectrum β-lactamases, ESBLs)检测等的结果,这些特殊的耐药表型可预示部分抗菌药物敏感性。
此外,报告还应该有微生物检验专业人员对报告结果的解释和评述(表5),使微生物检验报告在临床应用价值最大化。
加强临床微生物实验室与临床的沟通

加强临床微生物实验室与临床的沟通
3.2 咨询服务
咨询服务在CNAS-CL02:2012[12]文件中有相应的规定:(1) 为选择检验和使用服务提供建议,包括所需样品类型、临床指征和检验程序的局限性以及申请检验的频率;(2) 为临床病例提供建议;(3) 为检验结果解释提供专业判断;(4)推动实验室服务的有效利用;(5) 咨询科学和后勤事务,如样本不满足可接受标准的情况。微生物实验室的工作人员应参加临床会诊和疑难病例讨论,提供临床微生物专业解释,帮助临床确定真正的病原菌,尽可能为临床提供MIC的药敏报告,联合临床药师和感染科医师,结合药代动力学参数(Pharmacokinetic,PK)/药效动力学(Pharmacodynamics,PD),共同优化患者抗菌药物治疗的方案,提高微生物报告的有效利用。咨询服务的形式不局限于会诊与疑难病例讨论,应结合多种手段,包括电话咨询、医院OA系统(Office Automation)、定期对临床医护人员进行培训以及去临床科室走访等。
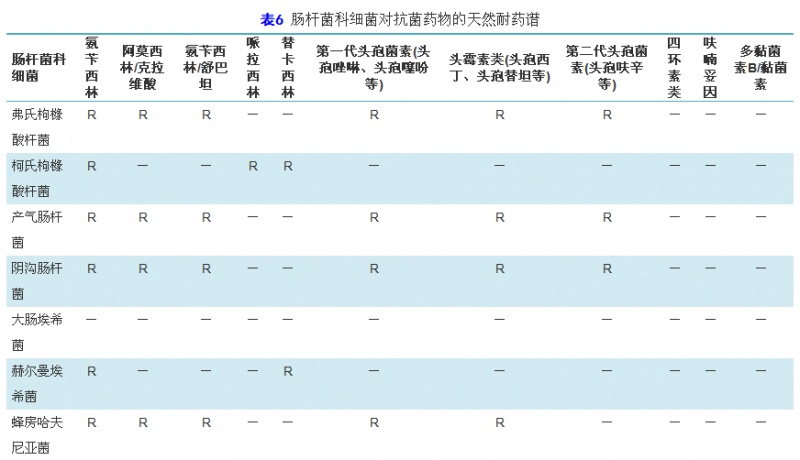
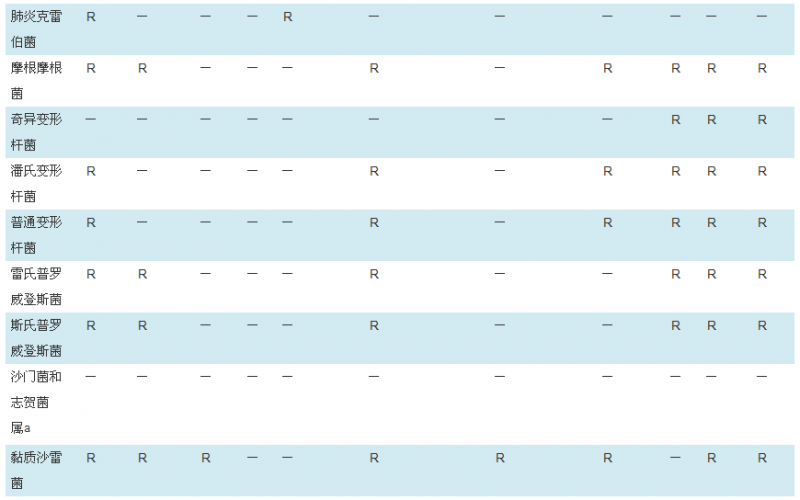
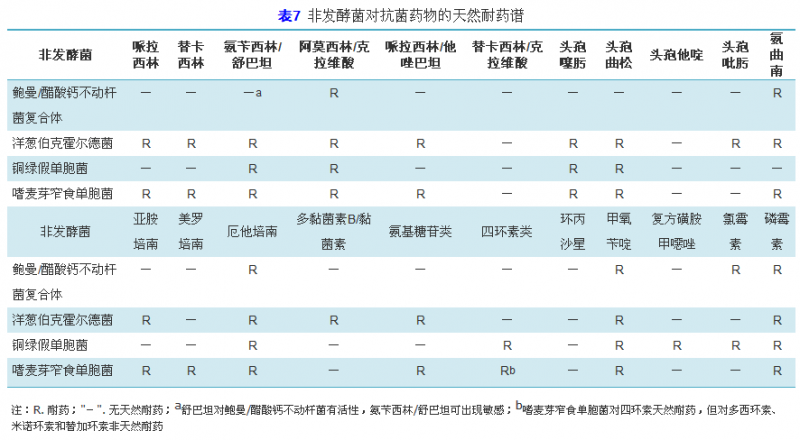
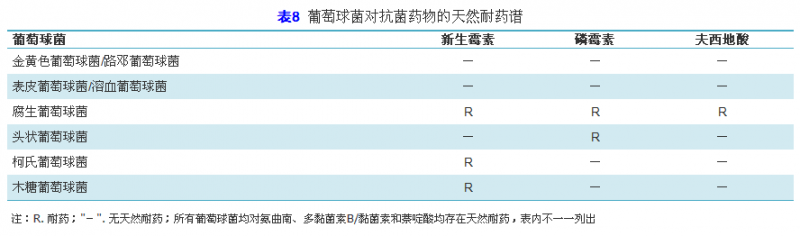
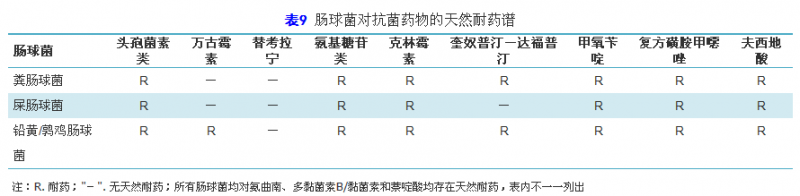
临床微生物工作人员在为临床提供药敏报告的同时,需要通过上述多种手段让临床医师了解临床常见病原菌的天然耐药谱。表6,表7,表8,表9是临床常见细菌的天然耐药情况[11]。其中,肠杆菌科细菌对克林霉素,达托霉素,夫西地酸,糖肽类(万古霉素、替考拉宁),利奈唑胺,大环内酯类(红霉素、克拉霉素、阿奇霉素),奎奴普汀-达福普汀,利福平天然耐药,对部分第一和第二代头孢类药物也存在天然耐药,而对第三代头孢类药物如头孢吡肟、氨曲南、替卡西林/克拉维酸、哌拉西林/他唑巴坦等和碳青霉烯类药物则不存在天然耐药。其中,大肠埃希菌、沙门菌和志贺菌属对β-内酰胺类药物无天然耐药,奇异变形杆菌对青霉素类和头孢类抗菌药物无天然耐药。非发酵革兰阴性菌也对第一和第二代头孢菌素、头霉素类、克林霉素、达托霉素、夫西地酸、糖肽类、利奈唑胺、大环内酯、青霉素、奎奴普汀-达福普汀和利福平天然耐药(表7)。革兰阳性菌对氨曲南、多黏菌素B/黏菌素和萘啶酸均存在天然耐药,其中,肠球菌属对头孢菌素类、氨基糖苷类(除高浓度氨基糖苷类耐药检测外)、克林霉素和复方磺胺甲噁唑可能体外显示活性,但临床无效,也不应报告敏感。存在天然耐药的这些药物不必进行药物敏感性试验,可作为评语或备注出现在报告中。
加强临床微生物实验室与临床的沟通
加强临床微生物实验室与临床的沟通
加强临床微生物实验室与临床的沟通

加强临床微生物实验室与临床的沟通
加强临床微生物实验室与临床的沟通
加强临床微生物实验室与临床的沟通
临床医师在了解天然耐药同时,需要与微生物实验室主动沟通,帮助实验室制定样本采集规范,商定抗菌药物药敏试验的范围,让实验室工作人员了解最新的感染诊治进展。临床科室需联合临床微生物检验工作人员、临床药师以及管理者进行抗菌药物的处方点评,对抗菌药物使用的患者情况、适应证、禁忌证、用药种类、用法、用量、取药量、相互作用、注意事项等进行逐一检查,规范临床抗菌药物的使用。
3.3 定期监测数据的发布
临床微生物室工作人员应至少每年将流行病学资料统计分析后报告给临床医师。如:(1)各种样本(代表各种感染部位)的病原菌分布,使临床医师了解本地区该类感染疾病的病原谱,有利于早期诊断,找出本科室的流行株,积极阻断耐药菌传播途径,降低医院感染发生率;(2)药敏结果的统计,这是临床医师初始治疗经验用药的依据,最好能够对近几年耐药变化趋势及MIC变化趋势进行统计。监测数据应同时向医院药事委员会(抗菌药物使用决策机构)汇报,根据数据调整抗菌药物适用范围及品规。
综上所述,临床微生物检测周期较长,微生物实验室与临床的积极沟通,能够帮助临床早期诊断,提高检测的准确性,有效避免抗菌药物的过度使用和滥用,减少或者延缓耐药的产生。临床与微生物实验室的沟通不仅仅是需要微生物检验的专家走出去,走向临床,也同样需要将临床医师请进实验室,包括临床药师、院感部门,多学科合作才能提高抗感染水平。
参考文献
[1]中华人民共和国国家卫生和计划生育委员会. 《抗菌药物临床应用管理办法》(卫生部令第84号)[EB/OL]. (2012-05-08)[2015-03-15]. http://www.moh.gov.cn/mohzcfgs/s3576/201205/54645.shtml.
[2]FlayhartD, BorekAP, WakefieldT, et al. Comparison of BACTEC PLUS blood culture media to BacT/alert FA blood culture media for detection of bacterial pathogens in samples containing therapeutic levels of antibiotics[J]. J Clin Microbiol, 2007, 45(3):816–821.
[3]TunkelAR, HartmanBJ, KaplanSL, et al. Practice guidelines for the management of bacterial meningitis[J]. Clin Infect Dis, 2004, 39(9):1267–1284.
[4]徐英春,倪语星,王金良. 血培养操作规范[M]. 1版. 上海:上海科学技术出版社,2002.
[5]KaditisAG, O'MarcaighAS, RhodesKH, et al. Yield of positive blood cultures in pediatric oncology patients by a new method of blood culture collection[J]. Pediatr Infect Dis J, 1996, 15(7):615–620.
[6]DellingerRP, LevyMM, RhodesA, et al. Surviving Sepsis Campaign: international guidelines for management of severe sepsis and septic shock, 2012[J]. Crit Care Med, 2012, 41(2):580–637.
[7]MahonCR, LehmanDC, ManuselisG, et al. Textbook of Diagnostic Microbiology[M]. 5th Ed. Elsevier, Inc, 2013.
[8]MurrayPR, BaronEJ, JorgensenJH. Manual of clinical microbiology[M]. 9th ed. Washington, DC: ASM Press, 2007.
[9]BaddourLM, WilsonWR, BayerAS, et al. Infective endocarditis: diagnosis, antimicrobial therapy, and management of complications: a statement for healthcare professionals from the Committee on Rheumatic Fever, Endocarditis, and Kawasaki Disease, Council on Cardiovascular Disease in the Young, and the Councils on Clinical Cardiology, Stroke, and Cardiovascular Surgery and Anesthesia, American Heart Association: endorsed by the Infectious Diseases Society of America[J]. Circulation, 2005, 111(23):e394–e434.
[10]CNAS-CL42医学实验室质量和能力认可准则在临床微生物学检验领域的应用说明[S]. 中国合格评定国家认可委员会,2012.
[11]Clinical and laboratory standards institute (CLSI). M100-S25 Performance standards for antimicrobial susceptibility testing;Twenty-thrid informational supplement[S]. PA, Wayne: CLSI, 2015.
[12]CNAS-CL02医学实验室质量和能力认可准则[S].中国合格评定国家认可委员会,2013. |
 |关于我们|医维基|网站地图|Archiver|手机版|医疗之家
( 沪ICP备2023001278号-1 )
|关于我们|医维基|网站地图|Archiver|手机版|医疗之家
( 沪ICP备2023001278号-1 )